Teknologier til unik udstyrsidentifikation automatiserer læsning af medicinsk ID og stregkoder
Bidraget af DigiKeys nordamerikanske redaktører
2023-10-26
I 2013 implementerede den amerikanske fødevare- og lægemiddeladministration, U.S. Food and Drug Administration (FDA), en regel vedrørende et system til unik identifikation af udstyr (Unique Device Identification System/UDI). Reglen havde til formål at forbedre patientsikkerheden ved at tilvejebringe en ensartet metode til sporing og identifikation af medicinaludstyr ved hjælp af moderne dokumentation på produktions-, distributions- og brugssteder. Ligesom reglerne vedrørende medicinaludstyr i Europa eller lignende regler i andre lande øger den amerikanske UDI-regel rapporteringens nøjagtighed og letter analysen i tilfælde af tilbagekaldelse eller utilsigtede hændelser.
Fra den 24. september 2023 vil FDA fuldt ud håndhæve den nationale sundhedsrelaterede varekode (National Health Related Item Code) og lægemiddelkodenumre (Drug Code Numbers) på udstyrsmærkater og -emballager. Alt medicinaludstyr, der mærkes på eller efter denne dato, skal fuldt ud overholde UDI-mandaterne. Dette mandat vil have indvirkning på følgende:
- Livskritiske produkter i klasse 3, såsom pacemakere og implanterede proteser
- Klasse 2 moderat kritiske produkter, såsom sprøjter, katetre og absorberbare suturer
- Klasse‐1-produkter med lavere risiko, såsom tandtråd, lægekitler og iltmasker
Mandatets fulde håndhævelse betyder, at hvis et medicinaludstyr ikke har en stregkode, der kan scannes, vil det ikke længere blive betragtet som et gyldigt/anvendeligt produkt, selv om der er menneskeligt læsbare mærkater på det, og selv om produktet generelt antages at være let at identificere for de fleste brugere. Denne fulde håndhævelse vil anspore den medicinske industri til at indføre omfattende regler for fakturering af sygesikring.
 Figur 1: Nogle håndholdte DPM-stregkodeverifikatorer har avanceret belysning og anden software, der automatisk finder symboler og cykler gennem indstillinger for at optimere læsningen af det specifikke DPM-mærke og materialesubstrat. Faktisk kan LVS-9585, som er vist her, verificere både DPM-dele og trykte mærkater til omfattende analyse og rapportering. (Billedkilde: Omron Automation)
Figur 1: Nogle håndholdte DPM-stregkodeverifikatorer har avanceret belysning og anden software, der automatisk finder symboler og cykler gennem indstillinger for at optimere læsningen af det specifikke DPM-mærke og materialesubstrat. Faktisk kan LVS-9585, som er vist her, verificere både DPM-dele og trykte mærkater til omfattende analyse og rapportering. (Billedkilde: Omron Automation)
Den ordregivende enhed (varemærkeindehaveren) er ansvarlig for
I USA er IP-ejeren og det brugervendte varemærke for hvert medicinaludstyr ansvarlig for UDI-kodernes nøjagtighed og kvalitet. Det er især vigtigt, fordi så stor en del af markedet for medicinske produkter er kontraktproduceret og outsourcet til andre organisationers produktionsanlæg. Derfor er det den kontraherende organisations ansvar at sikre, at hele dens forsyningskæde er UDI-kompatibel og producerer nøjagtige mærkater.
Oprindelser af unik teknologi til identifikation af udstyr
UDI'er er statiske udstyrsidentifikatorer. Ændringer i mængden af varer i en pakke kan imidlertid udløse behovet for en ny identifikator. De udstedende myndigheder dikterer, hvordan disse detaljer skal skelnes fra hinanden. På samme måde kan en ændring af sterilitetsbetingelserne for udstyrets emballage også ændre udstyrets identifikator. Ændring af et udstyrs destinationsmarked (det land, hvor en enhed vil blive solgt), mærkatets sprog eller CE-mærke kan også nødvendiggøre ændringer af udstyrsidentifikatoren.
Før UDI-reglerne blev indført, kunne en producent af medicinaludstyr have mærket et produkt med et bestemt varenummer. Distributøren ville ændre varenummeret, inden sundhedsudbyderen eller hospitalet ændrede det igen. Da alle organisatoriske enheder kunne ændre varenummeret, inden det nåede frem til patienten, var det næsten umuligt at spore produkter, håndtere tilbagekaldelser, forhindre forfalskninger eller bestille nye varer på en effektiv måde.
Relateret: Implementering af robuste sporbarhedsløsninger
Nu om dagen får alt udstyr en standardiseret og vedvarende identifikator, betegnet en UDI, så alt udstyr kan identificeres hurtigere og mere præcist hvilket i sidste ende reducerer medicinske fejl. Denne UDI er en alfanumerisk kode, der indeholder to vigtige data:
- En udstyrsidentifikator
- En produktionsidentifikator
En udstyrsidentifikator er en statisk mærkat, der tildeles et givet udstyr, og som angiver mærkatets udsteder (typisk udstyrets producent) og udstyrets specifikke modelnummer. Derimod indeholder en produktions-id data, der kan variere, og mange af de data, den kan indeholde, er valgfrie. Disse kan inkludere parti- og batchkoder, serienumre, udløbsdatoer og produktionsdatoer. Kort sagt kan de valgfrie data være alt, som en producent eller mærkatmager finder nødvendigt for at understøtte udstyrssporing.
Hver UDI-mærkat skal præsentere disse oplysninger i to former:
- Menneskeligt læsbar form (klar tekst)
- Maskinlæsbar form (kan læses af en stregkode- eller RFID-læser)
Når et udstyr kan anvendes til flere medicinske formål, skal UDI'en mærkes direkte på udstyret, ikke på emballagen. Reglen gælder også for udstyr, der kan bruges flere gange.
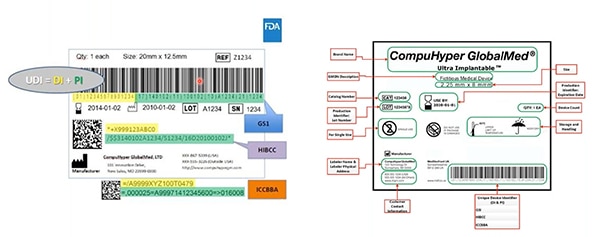 Figur 2: GS1, HIBCC og ICCBBA - UDI-udstedende agenturer - opretter UDI'er, tildeler tilladt symbologi til UDI'er, definerer hvilke teknologier der kan interface med UDI'er, og specificerer den krævede kvalitet af UDI-mærker. Udstyrsidentifikatoren er fremhævet med gult på dette eksempel; produktionsidentifikatorerne er fremhævet med grønt. Andre elementer inluderer menneskeligt læsbare oplysninger... og det er også kodet ind i den maskinlæsbare stregkode. (Billedkilde: FDA)
Figur 2: GS1, HIBCC og ICCBBA - UDI-udstedende agenturer - opretter UDI'er, tildeler tilladt symbologi til UDI'er, definerer hvilke teknologier der kan interface med UDI'er, og specificerer den krævede kvalitet af UDI-mærker. Udstyrsidentifikatoren er fremhævet med gult på dette eksempel; produktionsidentifikatorerne er fremhævet med grønt. Andre elementer inluderer menneskeligt læsbare oplysninger... og det er også kodet ind i den maskinlæsbare stregkode. (Billedkilde: FDA)
Alt udstyr skal registreres i den globale UDI-database for at kunne spores i tilfælde af en tilbagekaldelse og for at give offentligheden adgang til oplysninger om et givet udstyr. FDA-akkrediterede udstedende agenturer er autoriseret til at skabe unikke identifikatorer, som producenter af udstyr kan placere på deres produkter.
Relateret hvidbog: Hold dig opdateret om sporbarhed
UDI-scanningsteknologier og -teknikker
UDI-mærker kan verificeres på flere måder på deres vej fra fremstilling til brug.
On-line-verifikation udføres af teknologier, der er integreret i større maskiner til hurtig og præcis behandling af et stort antal produkter, mens de produceres. Understøttet af avanceret software tager disse teknologier lejlighedsvis form af labelprintere i industriel kvalitet. Disse printere er i stand til at foretage deres egen on-line-verifikation for at bekræfte, at UDI-oplysningerne er læsbare i henhold til de strenge industristandarder, umiddelbart efter oprettelsen på det sted, hvor labelen produceres. For eksempel er Omron Automation V275-verifikatorer til brug med Zebra termiske printere for at overholde ISO 15426 og udstedelsesmyndighedens GS1 -standarder for overholdelse af FDA's regler.
Relateret: Omrons løsninger til sporbarhed
Andre steder tager on-line-verifikation form af specialiseret maskine-vision, der flankerer transportbånd på automatiserede produktionslinjer, og som inkorporerer stregkodelæsning til ekstremt hurtig og præcis verifikation af UDI-mærkning på højhastighedsproduktionslinjer med mange forskellige produkter. Omron Automations MicroHAWK-produkter udmærker sig på dette område med avancerede sensorer suppleret med en miniaturiseret konstruktion og tilslutningsmuligheder, der inkluderer Ethernet/IP og PROFINET.
Relateret: Undgå erstatningsansvar for fejlagtig mærkning
Derimod er offline UDI-verifikation bedst egnet til batch-sampling af mærkater for at sikre kvaliteten. Offline-verifikationen bruges ofte til at teste prøver, når medicinaludstyr forlader eller ankommer til en enhed, og kan supplere online-verifikationssystemer opstrøms i distributionsforløbet.
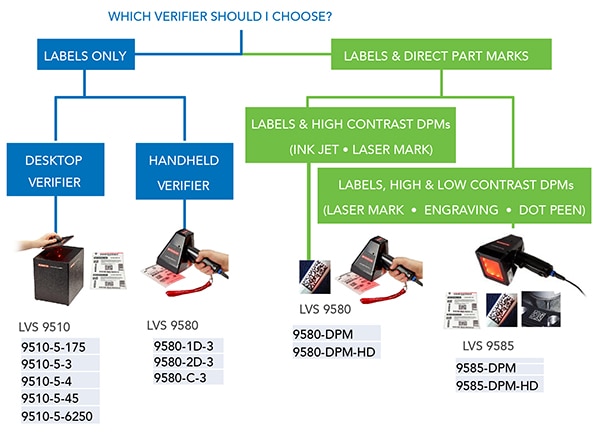 Figur 3: UDI'er, der er markeret direkte på produkter, kræver andre verifikatorer end dem, der bruges til UDI'er trykt på påsatte mærkater. (Billedkilde: Omron Automation)
Figur 3: UDI'er, der er markeret direkte på produkter, kræver andre verifikatorer end dem, der bruges til UDI'er trykt på påsatte mærkater. (Billedkilde: Omron Automation)
Faktisk kan alle medicinske distributions- og sundhedsaktiviteter drage fordel af at bruge ISO-kompatible verifikatorer. Overvej Omrons LVS 95XX-serie af offline UDI-verifikationsprodukter. Disse anvendes:
- på lasermarkeringsstationer og labelprintere, hvor der oprettes koder
- hvor koder anvendes på produkter, som måske eller måske ikke er adskilt fra det område, hvor koden oprettes
- i kvalitetskontrolstationer, hvor skabeloner, formatering og andre kodeelementer bekræftes
Specificering af offline variationer i UDI-verifikatorer
Hvilken offline UDI-verifikator der er bedst egnet til en given anvendelse, afhænger af flere parametre.
Stregkodens størrelse: Store stregkoder er ofte lettere at scanne med identifikatorer, der har et stort synsfelt defineret af objektivets brændvidde og sensorens størrelse. Et eksempel er Omron Automations LVS-9510-desktop-UDI-identifikatorer. Denne produktserie kan læse både lineære og 2D-mærkater. Fem forskellige versioner har hver sit synsfelt, så designere kan vælge den version, der er kompatibel med størrelsen på den stregkode, der skal verificeres. En stitching-funktion gør det muligt at sortere stregkoder, der overskrider synsfeltet.
Derudover kan alle LVS-9510'ere automatisk bestemme den symbologi og blænde, der er nødvendig for at evaluere koden og identificere og fremhæve problemområder.
 Figur 4: Stregkodeverifikation, der opfylder ISO-standarder, gøres lettere med udstyr, der kan verificere både lineære (1D) og todimensionelle (2D) koder. Noget af dette udstyr bestemmer den symbologi og blænde, der er nødvendig for at evaluere koder, og identificerer og fremhæver problemer. LVS-9510, der vises her, har en stitching-funktion, der gør det muligt at sortere stregkoder, der er større end synsfeltet. (Billedkilde: Omron Automation)
Figur 4: Stregkodeverifikation, der opfylder ISO-standarder, gøres lettere med udstyr, der kan verificere både lineære (1D) og todimensionelle (2D) koder. Noget af dette udstyr bestemmer den symbologi og blænde, der er nødvendig for at evaluere koder, og identificerer og fremhæver problemer. LVS-9510, der vises her, har en stitching-funktion, der gør det muligt at sortere stregkoder, der er større end synsfeltet. (Billedkilde: Omron Automation)
Stregkodetype: Scannere skal læse stregkodeformater som tildelt af de udstedende organer kendt som HIBCC, ICCBBA eller (mest almindeligt fra 2023) GS1. GS1 dikterer størrelse, format og opløsning for UPC'er, lineære stregkoder og 2D-datamatrix-stregkoder.
Placering af UDI-mærke: Tag for eksempel den direkte delmærkning (direct part marking/DPM) af medicinaludstyr. Disse markeringer kan være utroligt små, især når de identificerer kirurgiske instrumenter og implanterbart medicinaludstyr. For at læse og verificere sådanne DPM-UDI'er har Omrons LVS-9580 og LVS-9585 håndholdte verifikatorer med ultrahøj-densitet en specialiseret linse, der kan klassificere utallige DPM'er, herunder dem med cellestørrelser ned til 0,002”. Linser i industriel kvalitet inde i LVS-9580 og LVS-9585 sikrer konsistent læsenøjagtighed. De mest sofistikerede er de meget kontrollerbare og kalibrerebarer lysteknologier inde i scannerne. Sammen med flere synsfelter giver belysningen mulighed for øjeblikkelig optimering af de optagne UDI-billeder. Det er især vigtigt, fordi kodestandarden ikke tillader efterfølgende korrektioner eller billedmanipulationer.
Mere om UDI-scannersoftware
For at opnå maksimal effektivitet skal UDI-software, der understøtter verifikator-hardware, præsentere diagnostiske oplysninger i et intuitivt format. Denne software skal klassificere UDI-koder i henhold til ISO-definerede parametre (vigtigst af alt for at bekræfte deres læsbarhed) og bør ideelt set også spore forværrede problemer over en række UDI-scanninger.
Omron inkluderer al nødvendig software med hver eneste af deres UDI-scanningshardware. Softwaren opdateres regelmæssigt for at holde trit med de hurtigt udviklende regler og ny branchelovgivning.
En væsentlig funktion i Omrons scannersoftware er håndtering af kodesyntaks. Kort sagt skal hver stregkode eller 2D-kode nøjagtigt udtrække alle relevante oplysninger, herunder produkttype, partinummer, mængde, hvis det er relevant, udløbsdato, forsendelsesoplysninger osv. De resulterende datastrenge skal formateres på en bestemt måde for at holde trit med skiftende krav, metoder og destinationer for medicinale produkter.
Regelmæssigt opdateret software fra scannerproducenten sikrer, at slutbrugerne er opdaterede, selv når der udgives nye koder.
Konklusion
Det amerikanske militær havde engang et mål om fuldt ud at anvende et UID-produktsporingssystem, der lignede UDI-systemet i den medicinske industri. Formålet var at begrænse det enorme spild, der var forbundet med tabte, duplikerede og uoptalte forsyninger på militære installationer, herunder alt fra færdige Raytheon-våben til kontroltavler, leveret af en lille virksomhed til en eller anden specialiseret anvendelse. I dag bruges UID'ere på forskellige niveauer.
Det samme bliver ikke skæbnen for UDI-mandatet.
Mantraet bag indførelsen af UDI er ligetil: Mærkatet er produktet. Når alt kommer til alt, kan en forkert mærkat forårsage en kæde af begivenheder, der spilder sundhedspersonalets tid og resulterer i, at det medicinaludstyr bliver smidt væk. Derfor skal UDI'ere vises på alle lag af emballagen, f.eks. på enheds-, pakke-, bundt-, kasse- og palleniveau. UDI'er på sterilt medicinaludstyr inden i steriliseringsforseglinger er særligt vigtig, da det er uacceptabelt at bryde forseglingen for at verificere udstyrstypen.
Med FDA's krav om fuld overholdelse af UDI-direktiverne med virkning fra 24. september 2023 vil avancerede scanningsteknologier til verificering af medicinaludstyr blive altafgørende for automatiseringsproducenter såvel som for de maskinbyggere og slutbrugere, som de betjener.
Sådanne scannere kan opfylde ekstremt specifikke FDA UDI-krav for at bekræfte mærkater på en bred vifte af laboratorie-, medicinal- og klinisk diagnostisk udstyr. Offline stregkodeverifikatorer maksimerer sporbarhed, on-line-maskine-vision og avancerede DPM-læsere.

Disclaimer: The opinions, beliefs, and viewpoints expressed by the various authors and/or forum participants on this website do not necessarily reflect the opinions, beliefs, and viewpoints of DigiKey or official policies of DigiKey.






